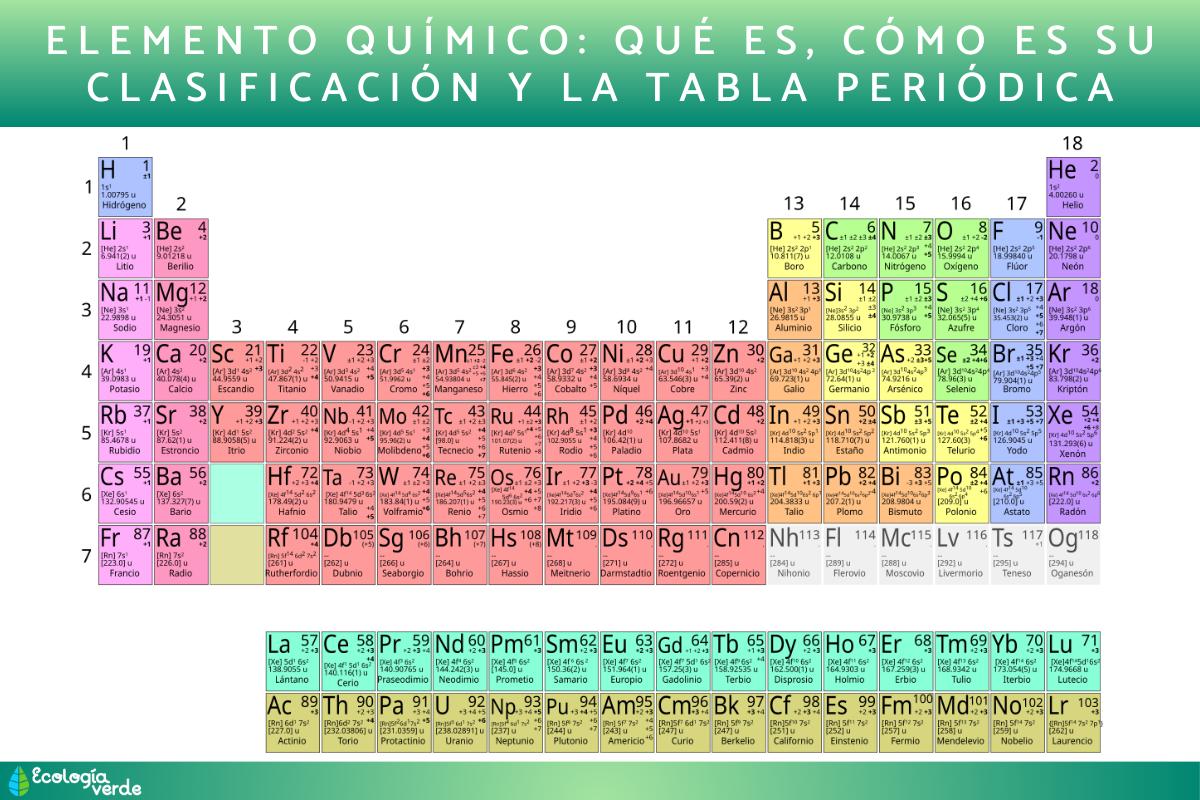
Un élément chimique est une substance pure composée uniquement d’atomes égaux (avec le même nombre de protons). Généralement, ils sont classés en métaux, non-métaux, métalloïdes, gaz rares et halogènes. Le tableau périodique organise les éléments en fonction de leur numéro atomique et de leur structure électronique. Ils sont disposés en périodes (lignes) et en groupes (colonnes), où ils partagent des propriétés chimiques dues au même nombre d’électrons de valence. Si vous souhaitez en savoir plus sur ce qu’est un élément chimique, sa classification et le tableau périodique, je vous invite à continuer la lecture de cet article d’Evidence Network.
Qu’est-ce qu’un élément chimique ?
Un élément chimique est compris comme une substance pure composée uniquement d’atomes identiques ou de même type. Contrairement aux mélanges et aux composés, les éléments ne peuvent pas être décomposés en substances plus simples par des processus chimiques ordinaires, comme l’indiquent les textes fondamentaux de chimie tels que ceux de Sánchez, García et Balderas.(1). Cette propriété essentielle en fait les composants fondamentaux de la matière. Dans le tableau périodique, chaque élément est identifié par un symbole spécifique et se distingue par son numéro atomique, qui représente le nombre de protons présents dans le noyau et définit ses propriétés.
Combien y a-t-il d’éléments chimiques ?
Le nombre d’éléments chimiques a progressivement augmenté. Il existe 118 éléments chimiques connus, dont 90 sont naturels et le reste synthétisé en laboratoire.(2). Les plus récents sont généralement radioactifs, avec une demi-vie courte et une stabilité difficile.
Comment sont classés les éléments chimiques ?
La classification des éléments est basée sur leur emplacement dans le tableau périodique et leurs propriétés physico-chimiques. Généralement, ils sont divisés en métaux, non-métaux et métalloïdes, tandis que les gaz rares et les halogènes forment des groupes particuliers.
Métaux
Les métaux constituent la famille la plus nombreuse du tableau périodique, située à gauche de la ligne en zigzag (sauf l’hydrogène). Ils se distinguent par leur brillance, leur conductivité, leur malléabilité et leur ductilité, en plus de former facilement des cations. Ils comprennent les alcalis, les alcalino-terreux, les transitions, les lanthanides et les actinides, avec une grande importance dans la construction, les câbles, l’électronique et la catalyse. Par exemple : l’or, l’argent, le fer, le cuivre, l’aluminium et le mercure.
Non-métaux
Les non-métaux se trouvent à droite du tableau périodique et se caractérisent par être de mauvais conducteurs, fragiles à l’état solide et présents dans divers états physiques. Ils forment des anions en gagnant des électrons, ont une densité et des points de fusion faibles, génèrent des oxydes acides et des oxyacides et sont essentiels à la vie en intégrant des composés organiques et inorganiques. Par exemple : l’oxygène, l’azote, le soufre et le carbone.
Métalloïdes
Les métalloïdes, situés sur la ligne zigzag du tableau périodique, ont des propriétés intermédiaires entre les métaux et les non-métaux. Ils comprennent le bore, le silicium, le germanium, l’arsenic, l’antimoine, le tellure et le polonium. Ils sont durs, cassants, avec un éclat semi-métallique et une conductivité intermédiaire. Ils se distinguent en tant que semi-conducteurs, le silicium étant fondamental dans les circuits intégrés et les appareils électroniques modernes. Par exemple : le silicium, le bore et l’arsenic.
gaz nobles
Les gaz rares, situés dans le groupe 18, sont monoatomiques, incolores, diamagnétiques et très peu réactifs en raison de leurs configurations électroniques stables. Généralement, ils ne forment pas de composés, bien que certains aient été synthétisés avec le xénon et le krypton. Ils ont des applications pertinentes : le néon est utilisé dans les publicités lumineuses et l’hélium, léger et ininflammable, dans les montgolfières. Par exemple : hélium, néon, argon, krypton, xénon et radon.
Halogènes
Les halogènes, groupe 17 du tableau périodique, sont des non-métaux hautement réactifs dont le nom signifie « générateurs de sel ». Ils forment des molécules diatomiques et des halogénures en se joignant aux métaux. Sa réactivité diminue avec l’augmentation de la masse atomique. On les trouve sous forme de sels naturels et sont utilisés dans la désinfection, l’oxydation, les médicaments et les polymères. Par exemple : le fluor, le chlore, le brome, l’iode et l’astatine.
Qu’est-ce que le tableau périodique et comment organise-t-il les éléments chimiques ?
Le tableau périodique organise les éléments en fonction de leur numéro atomique et de leur structure électronique. Créé par Mendeleïev en 1869 à partir de la masse atomique, il permettait d’anticiper des éléments inconnus. Dans sa version moderne, les éléments sont disposés en périodes (lignes) et en groupes (colonnes), où ils partagent des propriétés chimiques dues au même nombre d’électrons de valence.
- Périodes : le tableau comporte sept périodes. Dans les périodes longues (4 et 5) se trouvent les éléments de transition, tandis que les périodes 6 et 7 incluent les lanthanides et les actinides.
- Groupes : il y a 18 groupes ou familles. On distingue les métaux alcalins (1), les métaux alcalino-terreux (2), les halogènes (17) et les gaz rares (18). Chaque période commence par un métal alcalin et se termine par un gaz rare, montrant une transition du caractère métallique au caractère non métallique.
- Propriétés périodiques : à chaque période, le rayon atomique, l’électronégativité et l’énergie d’ionisation varient systématiquement, augmentant le caractère non métallique.
A quoi servent les éléments chimiques ?
- Industrie et technologie : les métaux tels que le fer, le cuivre et l’aluminium sont utilisés dans la construction, les machines et les câbles ; Le chrome est utilisé dans le chromage et le vanadium dans les alliages d’acier plus résistants.
- Santé et chimie du quotidien : les halogènes comme le chlore et l’iode sont indispensables à la désinfection et à la nutrition ; L’oxygène et le carbone sont essentiels à la respiration et à la biochimie.
- Technologie avancée : les métalloïdes tels que le silicium et le germanium s’imposent comme semi-conducteurs dans les circuits, les capteurs et les fibres optiques.
- Gaz rares : le néon éclaire les publicités et l’hélium est utilisé dans les ballons et la réfrigération cryogénique.
- Énergie et défense : les actinides tels que l’uranium et le plutonium soutiennent l’énergie nucléaire et les applications militaires.
Quelle est la différence entre un élément chimique et un composé chimique ?
La principale différence est que l’élément contient un seul type d’atome, tandis que le composé intègre différents atomes de différents éléments chimiques liés chimiquement.
Un élément chimique est une substance pure composée d’atomes du même type, indivisibles en substances plus simples par des processus chimiques communs ; Les exemples sont le fer, l’oxygène ou l’or. D’autre part, un composé chimique résulte de l’union chimique de deux ou plusieurs éléments dans des proportions fixes, acquérant des propriétés différentes de celles d’origine ; par exemple, l’eau et le chlorure de sodium. Les composés ont une formule chimique définie et ne sont pas facilement séparés par des méthodes physiques.
Si vous souhaitez lire plus d’articles similaires à Élément chimique : qu’est-ce que c’est, quelle est sa classification et le tableau périodique, nous vous recommandons d’entrer dans notre catégorie Autre environnement.
- Sánchez, J., García, M. et Balderas, Y. (2009). CHIMIE I. https://sacaba.gob.bo/images/wsacaba/pdf/libros/quimica/LibroQuimica.pdf
- Université nationale autonome du Mexique. (2019). Le tableau des éléments. https://www.universum.unam.mx/assets/temp/la-tabla-de-los-elementos/la-tabla-de-los-elementos-catalogo.pdf
- Contreras, R. (2019). Tableau périodique des éléments chimiques : cent cinquante ans d’histoire. Avancées en chimie, 14(1), 41-60. https://academiademerida.org.ve/wp-content/uploads/2019/06/RRContreras_Avances_Quimica_141-19_Periodic_Table.pdf
- Cabanne, D. et Fernández, A. (2014). CHAPITRE II : Classification périodique des éléments. https://www.fcf.unam.edu.ar/modules/uploads/2017/10/CAP%C3%8DTULO-II.pdf