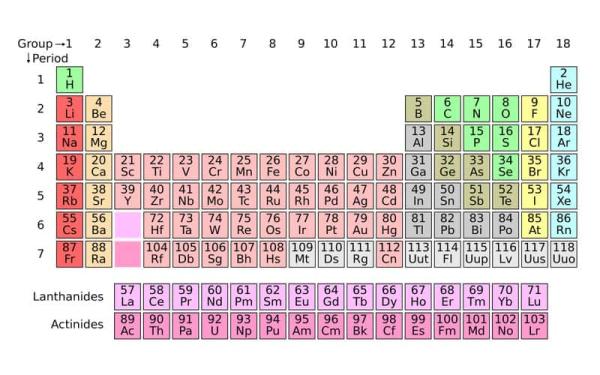
Le tableau périodique des éléments est un schéma sous forme de tableau qui montre de manière ordonnée et regroupée les différents éléments chimiques identifiés jusqu’à présent. Chaque élément contient dans sa case des informations sur son nombre de protons, sa configuration électronique et ses propriétés chimiques. Aujourd’hui, le tableau périodique contient 118 éléments.
Dans cet article de la BIOencyclopédie, nous vous expliquerons quelle est l’origine du tableau périodique, comment il est divisé et quelles caractéristiques des éléments chimiques sont inclus.
Histoire du tableau périodique
La première découverte scientifique d’un élément a été faite en 1669 par Hennig Brand, un chimiste allemand qui annonçait sa découverte du phosphore. À partir de là, le début de l’histoire du tableau périodique se consoliderait, puisqu’au cours des 200 années suivantes, d’autres éléments continuaient à être découverts. En 1869, un total de 63 éléments chimiques avaient déjà été identifiés et classés pour la première fois par le chimiste russe Dmitri Mendeleïev.
Mendeleev a développé la classification périodique des éléments. Lorsqu’il a entrepris d’organiser les éléments découverts jusqu’alors selon leur poids atomique, il a remarqué un modèle récurrent appelé « loi périodique », dans lequel les éléments appartenant au même groupe ou à la même colonne avaient des propriétés similaires.
Fort de cette connaissance, Mendeleev a fait de nombreuses prédictions sur de nouveaux éléments et compositions. En 1871, il présenta son deuxième tableau périodique amélioré avec quelques cases vides où, à un moment donné, les éléments à découvrir allaient avoir leur place. Actuellement, il continue d’être reconnu comme le fondateur du droit périodique.
Après la mort de Mendeleev, Henry Moseley a réussi à déterminer les valeurs expérimentales du numéro atomique de chaque élément, c’est-à-dire qu’il a trouvé un moyen de mesurer réellement le numéro atomique, ce que Mendeleev ne pouvait plus résoudre.
Certains livres désignent le chimiste anglais John Newlands comme le premier à dresser un tableau périodique. Eh bien, il a découvert qu’il y avait des similitudes entre des éléments dont les poids atomiques différaient de sept. Il a appelé cela « la loi des octaves » dans sa comparaison avec les octaves musicales et elle a été présentée dans un tableau qui, en raison de certains désaccords d’opinions, n’a pas été évalué.
Quatre ans plus tard, Mendeleïev dévoile son tableau et la société chimique reconnaît son travail, alors que ce n’est pas le cas de Newlands. Il faudra attendre 1998 pour que la société scientifique Société royale de chimie a reconnu sa précieuse contribution et son scoop.
Comment le tableau périodique des éléments est divisé
Le tableau périodique moderne est divisé en 18 colonnes et 7 périodes. Les lignes ou séries horizontales du tableau sont appelées périodes et les colonnes ou séries verticales sont appelées groupes.
Dans le tableau, quatre blocs différenciés sont reconnus : le bloc « s », le bloc « d », le bloc « p » et le bloc « f ». Chaque bloc contient des points. Le nombre de niveaux d’énergie d’un atome détermine la période à laquelle appartient un élément. Les périodes peuvent être : 1s, 2s, 3s, 4s, 5s, 6s, 7s, 4f, 5f, 3d, 4d, 5d, 6d, 2p, 3p, 4p, 5p, 6p et 7p.
Il est également possible de voir les divisions par couleur (la couleur choisie n’a pas d’importance) pour savoir à quel groupe ils appartiennent. Plus précisément, les éléments sont divisés en métaux, non-métaux et métalloïdes.
Métaux du tableau périodique
Les éléments classés comme métaux dans le tableau périodique sont répartis comme suit :
- Alcalin : Les métaux alcalins forment des alcalis en réagissant avec l’eau. Ils sont brillants et très réactifs à température et pression standard. Exemples : Lithium, Sodium et Potassium. Indiqué en rouge sur le tableau périodique.
- Terres alcalines : toutes se trouvent dans la nature et sont brillantes, argentées et non réactives à température et pression standard. Exemples : Magnésium, Calcium et Strontium. Montré en couleur crème sur le tableau périodique.
- Lanthanides : ceux-ci sont connus familièrement sous le nom d’éléments de terres rares, c’est pourquoi ils sont régulièrement affichés sous le corps principal du tableau. Exemples : Cérium, Samarium, Terbium. Montré en mauve sur le tableau périodique.
- Actinoïdes : ils sont importants pour leur radioactivité et plusieurs sont produits naturellement, mais la plupart sont artificiels. Exemples : Uranium, Plutonium, Curium. Montré en rose vif sur le tableau périodique.
- Métaux de transition : sont des éléments dont l’atome a une sous-couche « d » partiellement remplie à l’état métallique. Exemples : Titane, Cuivre, Zinc. Montré en rose clair sur le tableau périodique.
- Métaux du bloc P : ce sont des métaux mous à faible résistance mécanique et leurs points de fusion sont inférieurs à ceux des métaux de transition. Exemples : Aluminium, Gallium, Plomb. Indiqué en gris sur le tableau périodique.
Non-métaux du tableau périodique
Les éléments non métalliques du tableau périodique sont classés dans les groupes suivants :
- Autres non-métaux : ils sont très volatils et ne présentent pas les caractéristiques fondamentales des métaux telles que la dureté ou l’adaptabilité mécanique. Ils n’ont pas non plus la capacité de conduire l’électricité. Exemples : Carbone, Azote et Oxygène. Indiqué en vert sur le tableau périodique.
- Halogènes : Lorsqu’ils réagissent avec les métaux, ces éléments produisent des sels de sodium aux propriétés similaires. C’est le seul groupe qui contient des éléments dans les trois principaux états de la matière à température et pression standard. Exemples : Fluor, Chlore et Brome. Indiqué en jaune sur le tableau périodique.
- Gaz nobles : ce sont des gaz incolores, inodores, insipides et inflammables, en plus d’avoir une faible réactivation chimique. Exemples : Hélium, Néon, Xénon. Indiqué en bleu sur le tableau périodique.
Autres éléments du tableau périodique
Les métalloïdes sont des éléments dont les propriétés sont intermédiaires entre les métaux typiques et les non-métaux. Généralement, ce sont des solides cassants et quelque peu brillants qui, à température ambiante, sont des isolants électriques, mais qui, lorsqu’ils sont chauffés, sont des conducteurs électriques. Quelques exemples seraient le silicium, l’arsenic et le polonium, indiqués en vert olive dans le tableau périodique.
Boîtes d’éléments du tableau périodique
Dans chaque case du tableau périodique, il est possible de voir une série de nombres. Certains tableaux plus basiques montrent uniquement l’élément dont le numéro atomique est placé en haut à gauche, mais dans d’autres plus complets, vous pouvez lire plus d’informations sur l’élément. Regardons un exemple avec le Fer (Fe) :
- A gauche : masse atomique, énergie d’ionisation et configuration électronique.
- Sur le côté droit : numéro atomique, électronégativité et états d’oxydation.
Certains utilisent la numérotation IUPAC ou CAS, mais ce n’est pas une information aussi essentielle.
Si vous souhaitez lire plus d’articles similaires à Tableau périodique, nous vous recommandons d’entrer dans notre catégorie Biologie.
- http://www.rsc.org/periodic-table/history/about
- https://www.britannica.com/science/periodic-table-of-the-elements
- https://www.wou.edu/las/physci/ch412/perhist.htm